REVISIÓN BIBLIOGRÁFICA
Relationship between Cystatin C levels and the severity of kidney damage in patients with kidney failure
Relación entre los niveles de Cistatina C y la gravedad del daño renal en pacientes con insuficiencia renal
Alexandra Estefania Chugcho Aguagallo1
![]() *, Álvaro Paul Moina Veloz 2
*, Álvaro Paul Moina Veloz 2 ![]() *
*
1Universidad Técnica de Ambato. Facultad de Ciencias de la Salud, Carrera de Laboratorio Clínico. Ambato, Ecuador.
Citar como: Aguagallo AEC, Veloz ÁPM. Relación entre los niveles de Cistatina C y la gravedad del daño renal en pacientes con insuficiencia renal. Salud, Ciencia y Tecnología 2024;4:734. https://doi.org/10.56294/saludcyt2024734.
Enviado: 01-11-2023 Revisado: 18-12-2023 Aceptado: 08-01-2024 Publicado: 09-01-2024
Editor: Dr.
William Castillo-González ![]()
ABSTRACT
Introduction: renal failure is a disease in which the kidneys present a decrease in glomerular filtration, so they are not able to eliminate water and wastes from the blood correctly. It is classified into two types; acute kidney injury (AKI) and chronic kidney disease in which the latter has generated a greater impact in terms of mortality.
Objective: to relate Cystatin C levels and the severity of renal damage in patients with renal failure.
Methods: a descriptive and observational research was carried out with a non-experimental design and a descriptive and exploratory level of research, to develop this research the PRISMA methodology was used, where the main sources used for its development are detailed.
Results: this research describes the generalities about cystatin C, analytical methods, interferences, stability, and the stages of analysis of this biomarker, the same that was classified into pre-analysis, analysis and post-analysis of the test exposing in each of them the most important points involved.
Conclusions: cystatin C turns out to be a biomarker with a higher accuracy and sensitivity compared to other tests, in terms of clinical utility this test allows early detection of renal failure, and in patients suffering from this disease helps to determine the stage in which they are in this way allows to obtain a better diagnosis and prognosis regarding this condition.
Keywords: Renal Failure; Cystatin C; Glomerular Filtration Rate (GFR).
RESUMEN
Introducción: la insuficiencia renal es una enfermedad en la cual los riñones presentan un disminución del filtrado glomerular por lo que no son capaces de eliminar el agua y los desperdicios de la sangre de forma correcta. Se clasifica en dos tipos; insuficiencia renal aguda (IRA) e insuficiencia renal crónica (IRC) en la cual la segunda ha generado un mayor impacto en cuanto a la mortalidad que presenta.
Objetivo: relacionar los niveles de Cistatina C y la gravedad del daño renal en pacientes con insuficiencia renal.
Métodos: se realizó una investigación de tipo descriptiva y observacional con un diseño no experimental y un nivel de investigación descriptivo y exploratorio, para desarrollar esta investigación se llevó a cabo la metodología PRISMA donde se detallan las fuentes principales utilizadas para el desarrollo de este.
Resultados: en esta investigación se describen las generalidades sobre la cistatina C, los métodos analíticos, interferencias, estabilidad, y las etapas de análisis de este biomarcador, el mismo que se clasifico en preanálisis, análisis y post análisis de la prueba exponiendo en cada uno de ellos los puntos más importantes que conllevan.
Conclusiones: la cistatina C resulta ser un biomarcador con una exactitud y sensibilidad mayor en comparación a otras pruebas, en cuanto a la utilidad clínica esta prueba permite detectar precozmente la insuficiencia renal, y en pacientes que padecen esta enfermedad ayuda a determinar el estadio en el que se encuentran de esta forma permite obtener un mejor diagnóstico y pronóstico en cuanto a esta condición.
Palabras clave: Insuficiencia Renal; Cistatina C; Tasa de Diltrado Glomerular (TFG).
INTRODUCCIÓN
La insuficiencia renal es una enfermedad en la cual los riñones presentan un disminución del filtrado glomerular por lo que no son capaces de eliminar el agua y los desperdicios de la sangre de forma correcta.(1,2) Se clasifica en dos tipos; la insuficiencia renal aguda (IRA) es caracterizada por el deterioro acelerado de la función renal, es potencialmente reversible por lo que las personas con esta enfermedad pueden recuperarse con un tratamiento adecuado,(3,4,5) y la insuficiencia renal crónica (IRC) es aquella enfermedad donde se genera un daño estructural o funcional del riñón en un lapso mayor a tres meses,(6,7) suele evolucionar con el pasar de los años, además puede desencadenar en una insuficiencia renal total.(8)
La ERC ha generado un gran impacto debido a la mortalidad que presenta, en el año 2019 la Organización Mundial de la Salud (OMS) posicionó a las enfermedades renales en el puesto número diez dentro de las causas de mortalidad en la población a nivel mundial,(9) y en el año 2020 el Instituto Nacional de Estadística y Censos (INEC) ubicó a las enfermedades del sistema urinario en Ecuador en el puesto número ocho como causa de mortalidad en general en la población ecuatoriana, por delante de ella se encuentran las enfermedades cerebrovasculares y posterior los accidentes de transporte terrestre.(10)
En cuanto a su prevalencia en el año 2020 la OMS reportó en su base de datos que alrededor del 10 % de la población mundial presentó ERC,(11) en Latinoamérica el 6,83 % de la población general fue afectada por esta enfermedad,(12) mientras que en Ecuador se estima que esta enfermedad afectó a la población adulta de nuestro país en un 11 %,(7) además en el año 2022 a partir de datos recolectados por el INEC se registró 457 personas fallecidas a causa de la ERC en establecimientos de salud tanto públicos como privados.(13)
Por otra parte dentro de los criterios diagnósticos para determinar IRA se encuentran variaciones en los niveles de creatinina sérica, la producción de orina o las dos.(14) Y para realizar el diagnóstico de ERC mayormente se utilizan pruebas como la creatinina, urea, albúmina, electrolitos y la cistatina C,(15) por lo que la detección temprana de esta patología sería útil para prolongar la vida funcional de los riñones y la disminución de casos de diálisis.(16)
En la actualidad la Cistatina C ha generado interés como prueba para evaluar la función renal debido a que sus valores oscilan en relación con la variación de la tasa de filtrado glomerular (TFG).(17) Este biomarcador no suele afectarse por la edad, raza, sexo o masa muscular,(5) por ello se piensa que se puede desarrollar un marcador con mayor fiabilidad relacionado con la función renal de igual manera generaría una mejor exactitud debido a que presenta una mayor sensibilidad, de esta forma permitiría su diagnóstico en estadios iniciales.(18)
El objetivo de la presente revisión bibliográfica es relacionar los niveles de Cistatina C y la gravedad del daño renal en pacientes con insuficiencia renal a partir de la indagación de información con evidencia científica de los últimos cinco años referente a esta enfermedad, el impacto con el que se presenta esta patología tanto a nivel nacional como mundial, los métodos usados actualmente para su diagnóstico y los nuevos estudios que se han realizado para evidenciar el mejor biomarcador para un diagnóstico temprano y un tratamiento adecuado.
MÉTODOS
Para el presente artículo de revisión bibliográfica enfocado en la relación entre los niveles de Cistatina C y la gravedad del daño renal en pacientes con insuficiencia renal se realizó una revisión sistemática de estudios descriptivos y observacionales, con un objetivo descriptivo y exploratorio.
Usando el método Prisma.
Criterios de inclusión
· Tipo de estudio: ensayos clínicos y revisiones sistemáticas enfocados en la relación entre los niveles de Cistatina C y la gravedad del daño renal
· Rango de publicación: se optó por artículos publicados en el periodo del 2018-2023.
· Idioma de los artículos: artículos en inglés y español.
Criterios de exclusión
· Artículos con información insuficiente o irrelevante.
· Artículos sin relación al tema.
· Artículos publicados de forma anónima.
La búsqueda de información se realizó en bases de datos como: Google Académico, PubMed, Scopus, Redalyc. Para realizar la búsqueda los términos utilizados fueron: insuficiencia renal, cistatina C, tasa de filtrado glomerular (TFG). (Ver Figura 1).
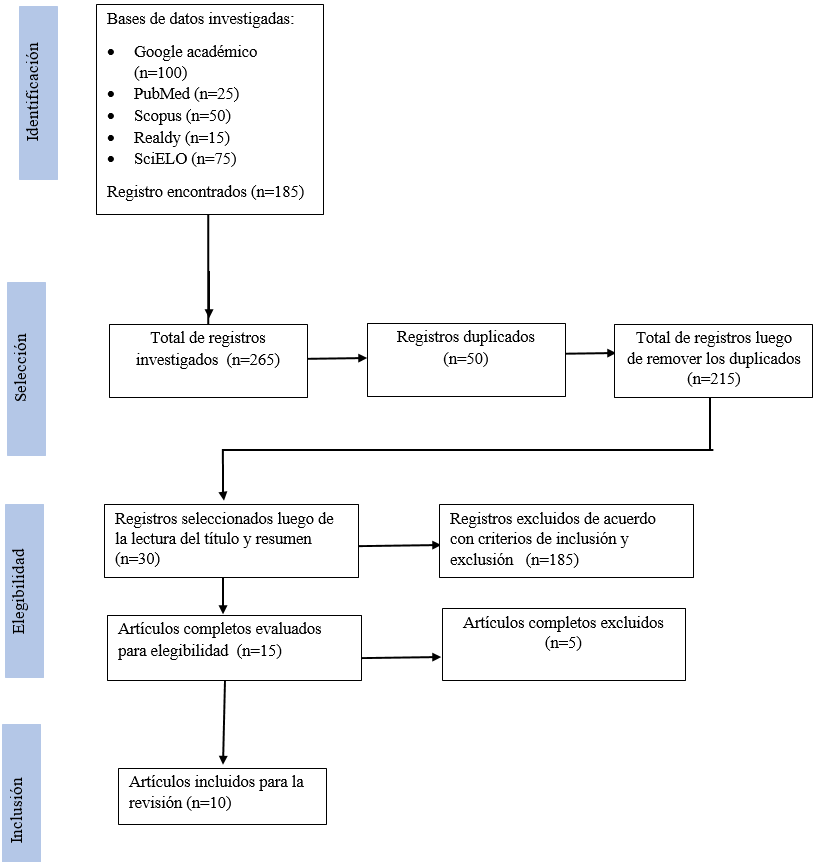
Figura 1. Flujograma utilizado para la búsqueda bibliográfica, basado en la metodología PRISMA
|
Tabla 1: Bibliografía referente |
|||||
|
Autor |
Año |
Titulo |
Metodología |
Resultados |
Conclusiones |
|
Legton & Mendoza.(17) |
2023 |
Cistatina c, urea y creatinina como indicador pronóstico de daño renal |
Investigación de tipo documental, y el estudio es de tipo descriptivo enfocado a la cistatina c, urea y creatinina como indicador pronóstico de daño renal
|
Dentro de Latinoamérica, la creatinina nos indica que valores >1,14 mg/dL, la urea >43,5mg/dL y la Cistatina C >0,103 mg/dL ya existe una presencia de daño renal. |
La detección inicial del daño renal suele realizarse por un aumento en los niveles de urea/creatinina, aunque la alteración de los niveles de cistatina C en el filtrado glomerular aún es discutible sin embargo, parece este biomarcador predice mejor el riesgo renal y la mortalidad que la creatinina. |
|
Alcívar J, Puig C, Wong J & Flor M.(21) |
2021 |
Determinación de Cistatina C como marcador de función renal en pacientes normoalbuminúricos con Diabetes Mellitus tipo 2. Estudio Multicéntrico. |
Estudio transversal observacional a 115 pacientes diabéticos tipo 2 normoalbuminúricos, estableciendo la tasa de filtrado glomerular con valores de cistatina C y fórmula de Cockroft–Gault.
|
Con cistatina C la tasa de filtrado glomerular fue de un valor promedio de 99 ± 19,07 ml/min, mientras que la de Cockroft-Gault un valor de 79,85 ± 23,63 ml/min, reflejando mejor correlación con aclaramiento de creatinina en orina de 24 horas que obtuvo un valor de 74,95 ± 37,41 ml/min. |
La tasa de filtrado glomerular con cistatina C presenta una gran dispersión en la correlación con el aclaramiento de creatinina en orina de 24 horas; este hecho, junto a diversos factores que influyen en su variabilidad.
|
|
Coronado Y.(22) |
2022 |
Cystatin C and Creatinine: renal function markers in patients treated with Cisplatin at the «Celestino Hernández Robau» University Hospital |
Investigación de desarrollo, descriptivo, longitudinal, prospectivo, a 60 pacientes con neoplasia de cabeza, cuello y pulmón, atendidos en el Hospital Universitario Oncológico “Dr. Celestino Hernández Robau” de Villa Clara en el periodo de abril de 2018 a abril de 2019. |
Los valores de · Creatinina: aumento con el transcurso de la quimioterapia · Cistatina C: en los pacientes con cáncer de cabeza y cuello se elevó por encima de los valores de referencia después de la quimioterapia |
Existió una correlación significativa, lineal, fuerte, positiva entre las concentraciones de creatinina y cistatina C y entre el ritmo de filtrado glomerular estimado con las fórmulas de Cockcroft-Gault y Hoek.
|
|
Díaz M, Berlis L, Robalino M & Proaño S.(7) |
2018 |
Epidemiological behavior on patients with terminal chronic kidney disease from Ecuador |
Estudio transversal en 84 pacientes con enfermedad renal crónica terminal ERCT, en tratamiento de hemodiálisis, en la clínica DIALVIDA Ambato, Ecuador.
|
Causas principales de ERCT: hipertensión arterial (23,8 %) y la diabetes mellitus (30,9 %), donde esta enfermedad predominó en el sexo masculino (63,1 %), en adultos mayores a 60 años (52,4 %), con normopeso (51,2 %), fumadores (47,6 %) y con bajo nivel de instrucción.
|
La ERCT, predominó en el sexo masculino, en adultos mayores normopeso, no fumadores, y con bajo nivel de instrucción. Las dos primeras causas fueron: diabetes mellitus e hipertensión arterial. |
|
Gahona J, Reyes P, Prado A, Meza K & Benítez C.(13) |
2023 |
Description and analysis of the incidence and prevalence rates of patients on renal replacement therapy in Ecuador |
Estudio cuantitativo transversal, utilizando los resultados obtenidos mediante el análisis de los datos proporcionados por el Registro Ecuatoriano de Diálisis y Trasplante Renal (REDT) con el programa estadístico stata versión 15, corte mayo-noviembre del 2022. |
Edad (años): · 0-18 · 19-45 · 46-70 · 71-100 Tasa de incidencia/100 000 habitantes · 0,8 · 3,3 · 28,2 · 111 Tasa de prevalencia/100 000 habitantes · 8,53 · 47,6 · 331,7 · 776,3 |
Se concluye que el rango etario en el Ecuador con mayor tasa de incidencia de prevalencia e incidencia es desde los 46-70 años y desde los 71-100 años. |
|
González Y, Carrazana M, Pérez L & Alemán A.(33) |
2022 |
Cistatina C como marcador precoz de daño renal en pacientes con Diabetes Mellitus II |
Investigación observacional, descriptivo de corte Transversal y correlacional en una muestra de 104 pacientes con diagnóstico de diabetes mellitus tipo 2 atendidos en el servicio de Laboratorio Clínico del Hospital Universitario “Arnaldo Milián Castro” de Santa Clara, Villa Clara. |
El grupo de edad de 40 a 49 años fue el más frecuente, prevaleciendo el sexo masculino donde se registraron los siguientes resultados microalbuminuria: 48 % valores normales de creatinina: 84,6 %. Cistatina C: 96,1 %
|
La cistatina C sérica resulta ser un marcador precoz de Enfermedad Renal Crónica en sus diferentes estadios. |
|
Reyes D.(12) |
2022 |
Renal profile and lifestyle in latin American |
Investigación de diseño documental de tipo exploratorio, descriptivo y bibliográfico enfocado en el perfil renal y estilo de vida en adultos de américa latina. |
Prevalencia de la enfermedad renal en América Latina · Uruguay 50,1 % · Cuba el 46,8 % · Bolivia un 44,3 % Colombia 41,33 % · Honduras 35 % · Paraguay 17 % · Perú 16 % · México 10 % · El Salvador 3,9 % |
El daño renal en América latina es alto, con mayor predominio es Uruguay presenta el 50,1 %, considerado un importante problema de salud mundial y más común en personas adultas.
|
|
Rosell, Gil, Herrera, Reyes & Rosell(29) |
2022 |
Cystatin c: useful marker in renal damage in pathologies and/or by the use of drugs |
Se realizó una revisión bibliográfica sistemática compilando información acerca de la utilización de la determinación de la Cistatina C como marcador precoz de daño renal, su importancia clínica en el uso de fármacos nefrotóxicos, y en algunas patologías. |
Los niveles de cistatina C en suero parecen ser una herramienta útil para la identificación de niños con reducción del FG (elevada sensibilidad) y para la exclusión de niños con FG normal (elevada especificidad). |
Se identificaron evidencias que esclarecen la utilidad de cistatina C como parámetro de medición del filtrado glomerular comparado con la creatinina en diferentes patologías y con el uso de fármacos que ocasionan daño renal. |
|
Soledispa W.(4) |
2022 |
Acute renal failure and risk factors in patients with Covid – 19 |
Investigación con un diseño narrativo documental de tipo descriptivo enfocado en la insuficiencia renal aguda y factores de riesgo en pacientes covid – 19. |
Factores de riesgo en pacientes que presentaron solo covid-19: · Hipertensión arterial (49 %) · E.cardiovascular (36 %) · Diabetes mellitus (34 %).
|
Se puede concluir en los hallazgos histológicos más frecuentemente observados en paciente COVID- 19 con insuficiencia renal aguda son: necrosis tubular, daño endotelial, agregados eritroides capilares, trombos de fibrina intracapilares glomerulares y signos inflamatorios. |
|
Solís M, Benavides G, Vásconez E & Campoverde A.(18) |
2020 |
Correlation cystatin “C” and serum creatinine regarding to glomerular filtration in patients with diabetic nephropathy. |
Estudio descriptivo, transversal. De una población de 418 se seleccionó una muestra de 124 datos de Historias Clínicas. Se analizaron los datos de resultados de medición de la cistatina C y creatinina sérica frente al filtrado glomerular de pacientes con Nefropatía Diabética en el período de junio a diciembre de 2017. |
La cistatina C vs la creatinina sérica frente al filtrado glomerular presentaron una correlación de 92 % (114; 124) y 66 % (81; 124) de forma respectiva, se obtuvo una mayor correlación con la cistatina C y una estrecha significancia bilateral de 0,00. |
La cistatina C y la creatinina sérica mostraron una alta correlación con el filtrado glomerular en pacientes con Nefropatía Diabética, la principal fue la cistatina C que detectó cambios precoces en el filtrado. |
|
Tabla 2: Principio, método y procedimiento para la medición de cistatina C |
|||
|
Principio |
Método |
Procedimiento |
|
|
Inmunoensayo turbidimétrico |
PETIA ( particle-enhanced turbidimetric immunoassay) |
Se genera una reacción entre la cistatina C y partículas de látex anti-cistatina C, por lo que en la muestra se genera un cambio en la absorbancia proporcional en cuanto a la cantidad de cistatina C.(23) |
|
|
Inmunoensayo nefelométrico |
PENIA (particle-enhanced nephelometric immunoassay |
Se forman complejos inmunes dando como resultado la dispersión de luz, a partir de ello la concentración de cistatina C obtenida de la muestra puede compararse con una curva de calibración establecida.(24) |
|
DESARROLLO
En 1961 la cistatina C fue descrita por primera vez en líquido cefalorraquídeo llamada proteína γ-traza, esta es una proteína sérica no glicosilada que pertenece a la familia 2 de la superfamilia de las cistatinas, presenta un peso molecular bajo de 13,3 kDa y está formada por una cadena de 120 aminoácidos y 2 puentes disulfuro (19).
Su filtración se lleva a cabo en los glomérulos, su reabsorción y metabolización ocurre en los túbulos renales, y se produce en todas las células nucleadas del organismo, la determinación del nivel sérico que presenta depende del índice de filtración glomerular.(20,21) En la cistein-proteasa actúa como un inhibidor endógeno además se encuentra presente en la mayoría de los fluidos corporales especialmente en líquido cefalorraquídeo, leche y plasma seminal.(20)
MÉTODOS ANALÍTICOS
En 1979 Löfberg y Grubb desarrollaron el primer método de medida de cistatina C en fluidos biológicos, el cual estuvo basado en una técnica cuantitativa denominada inmunodifusión radial simple que presentaba un 0,3 mg/L en el límite de detección y un 11 % en el coeficiente de variación intraensayo.(22)
Por otra parte en 1994 fueron desarrollados los primeros métodos automatizados para la medición de cistatina C (Ver tabla 2).
Los valores de referencia séricos para la cistatina C son de 0,58 a 0,92 mg/L y actualmente PENIA es el método de elección debido a que presenta una mayor sensibilidad de 83,3 % y especificidad de 79,2 % además de ser aprobado por la FDA (Federal Drug Administration).(22,25)
Interferencias
Entre las causas que puede generar interferencias endógenas en la cistatina C se encuentra lipemia >1000 mg/dl, bilirrubina >60 mg/dl, o condiciones patológicas del paciente como estados de disfunción tiroidea en la cual se presentan concentraciones elevadas de cistatina C en hipertiroidismo y en hipotiroidismo ocurre una disminución.(26)
Por otra parte dentro de las interferencias exógenas para este analito se encuentra el empleo de fármacos como corticosteroides, en el caso de la dexametasona podría generar una elevación del 80 % tras 48 horas de tratamiento, esto se debe a un incremento del promotor que participa en el gen de la cistatina C durante la transcripción.(27)
Además diferentes estudios manifiestan que en tumores como el cáncer colorrectal, mieloma múltiple y melanoma metastásico existe una elevación en la concentración de cistatina C alrededor de un 50 %.(27,28)
Estabilidad
Los ciclos de congelación y descongelación de la cistatina C no suele afectar su estabilidad, por lo que en suero a temperatura ambiente presenta una estabilidad de 2 días, a 4 ºC 1 semana, a -20 ºC de 1-2 meses y alrededor de 6 meses a -80ºC.(29)
Etapas para el análisis de cistatina C
Preanálisis: estas actividades empiezan a partir de la solicitud de los exámenes, la identificación y preparación del paciente, la toma de muestra, almacenamiento y transporte de muestras hasta su entrega en la respectiva área analítica.(30)
Por ello guías como el Procedures for the Collection of Diagnostic Blood Specimens by Venipuncture-Clinical and Laboratory Standards Institute (CLSI GP41-A7) mencionan algunas recomendaciones en esta etapa:
· Indicaciones previas a la toma de muestra: Se debe verificar la identidad del paciente y las pruebas que se realizará, en el caso de la cistatina C el paciente debe cumplir con ciertas condiciones para realizarse la prueba (Ver tabla 3).
|
Tabla 3: Condiciones de ayuno para el análisis de cistatina C |
|
|
Edad |
Ayuno |
|
Adultos |
Mínimo: 8 horas Máximo: 12 horas |
|
Niños de 0-1 años |
Mínimo: 2 horas |
|
Niños de 1-6 años |
Mínimo 4 horas |
Así mismo se toma en cuenta el estado del paciente como la dieta, ingesta de líquidos o medicamentos y el ayuno prolongado debido a que podrían alterar los resultados clínicos de forma relevante.(31)
· Instrucciones para realizar la toma de muestra: para realizar la prueba de cistatina C el flebotomista debe tener previamente listos los materiales necesarios que utilizará en esta etapa, se debe tomar en cuenta la posición del paciente por seguridad y para una buena obtención de la muestra, así mismo se verificará el sitio de punción con la ayuda del torniquete elástico el cual será colocado sobre el lugar de punción seleccionado aproximadamente a 7,5cm, sin exceder el tiempo establecido (1min), se realizara la asepsia con alcohol etílico al 70 % y con algodón realizando movimientos circulares de dentro hacia fuera en el sitio escogido sin repalpar para evitar contaminación, se procederá a realizar la venopunción y tomar la muestra en un tubo de tapa amarilla con gel separador, una vez obtenida la muestra es necesario evitar que el paciente doble el brazo con presión.(31)
· Transporte de la muestra: la muestra será transportada por el personal de salud en un contenedor cerrado o gradillas aplicando las medidas de bioseguridad respectivas, en el caso de realizar un envío externo de la muestra de cistatina C se deberá llevar a cabo el sistema triple básico para embalaje el cual consiste en 3 capas:(32)
Ø Empaque primario: es el recipiente que contiene la muestra, debe ser hermético y etiquetado correctamente con el nombre del analito, además tiene que ser envuelto en material absorbente para evitar derrames en caso de una rotura.(32)
Ø Empaque secundario: protege en su interior al empaque primario, así mismo debe contar con las características del primero y debe evitar la agitación o el choque de las muestras que contiene.(32)
Ø Empaque terciario: debe proteger al recipiente primario y secundario con el fin de evitar daños en la muestra durante su transporte, debe ser resistente y por ello se considera la composición, peso y tamaño de los empaques anteriores.(32)
· Centrifugación: a temperatura ambiente la centrifugación de la cistatina C se debe realizar con una fuerza de gravedad de 1 300 g previo a ser analizada, además para realizar la verificación de la centrifuga es necesario que el equipo cuente con una calibración adecuada la misma se realiza con la ayuda de tacómetros ópticos que permiten verificar con precisión la velocidad rotatoria del equipo.(33) (Ver tabla 4).
|
Tabla 4. Conversión de RPM a FG |
|
|
Revoluciones por minuto del rotor (RPM) |
3500 |
|
Radio del rotor (cm) |
10 |
|
Fuerza centrífuga relativa (RCF) o fuerza g |
1300 g |
Así mismo se toma en cuenta la recepción de la muestra, manipulación, preparación y almacenamiento previos al análisis.(34)
Análisis: la guía Statistical Quality Control for Quantitative Measurement Procedures: Principles and Definitions (CLSI C24) menciona que en este proceso se debe implementar la planificación de la calidad estructurada, por ello en la prueba de cistatina C es necesario una adecuada selección del procedimiento de medición, definición de requisitos de calidad, selección del control de calidad, establecimiento de medias y desviaciones estándar, abordaje de metas de calidad, verificación y validación de los procedimientos analíticos, la incertidumbre de medida, los intervalos de referencia biológicos y documentación de los procesos analíticos.(34)
Para mantener el aseguramiento en cuanto a la calidad de los resultados obtenidos del análisis se toma en cuenta los siguientes puntos:
· Calificación del equipamiento de medición: este proceso verifica que el equipo opere y sea instalado de forma correcta para asegurar que las futuras operaciones sean confiables y se encuentren dentro de los límites establecidos.(35)
· Calificación de equipos
Ø Calificación de diseño: detalla las especificaciones operacionales y funcionales del equipo así como requerimientos establecidos por el fabricante.(35)
Ø Calificación de instalación: En esta etapa se verifica que el equipo analítico está instalado correctamente en el ambiente seleccionado y con las especificaciones correctas.(35)
Ø Calificación de operación: se demuestra que el equipo funciona correctamente acorde a la especificación operacional en el ambiente previamente seleccionado.(35)
Ø Calificación de desempeño: En este punto se verifica que el equipo analítico se desempeña de acuerdo con lo establecido por el fabricante en términos de aseguramiento de especificaciones de desempeño analítico de acuerdo con el uso previo.(35)
· Verificación del desempeño analítico: En la guía “User Verification of Precision and Estimation of Bias,” (CLSI EP 15A3C) se recomienda a los laboratorios verificar las especificaciones de desempeño para el uso previsto de acuerdo con el fabricante y el uso clínico, la prueba de cistatina C se realiza a partir de un método cuantitativo por lo que para verificar su desempeño analítico se requiere de protocolos de verificación o validación para el mismo.(36)
· Planificación del sistema de gestión de calidad: Es necesario para validar y establecer procesos que satisfacen las necesidades de los pacientes, por ello se debe contar con varios mecanismos de control y técnicas preventivas que permita monitorear el proceso total del análisis de la cistatina C (Ver figura 2).
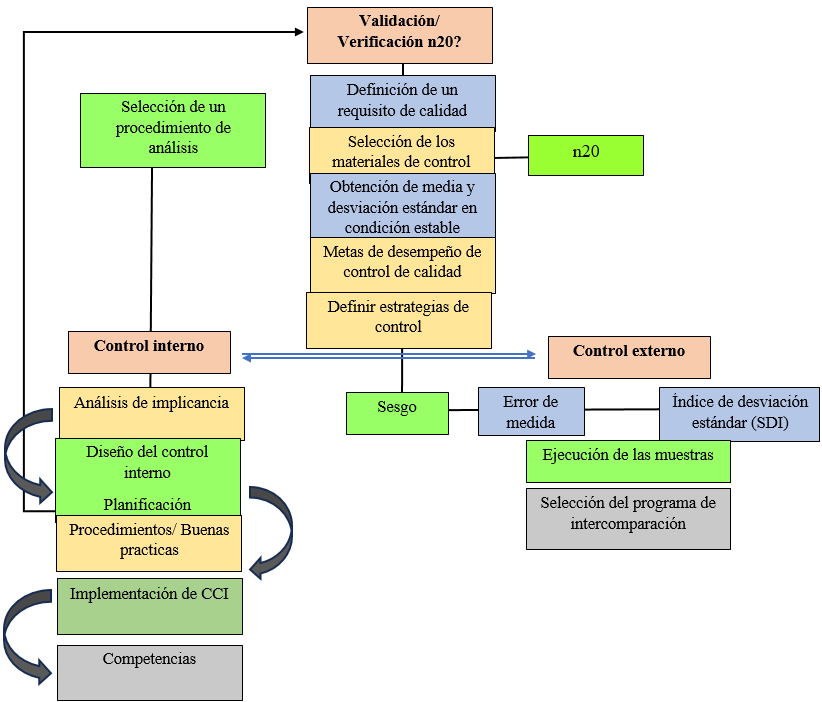
Figura 2. Planificación del sistema de gestión de calidad
· Seleccion de procediemto
Ø Definición de requisitos de calidad: la ISO 9001:2015 menciona que el laboratorio debe implementar, planificar y determinar los respectivos procesos de seguimiento, análisis, mejora y medición para demostrar la conformidad de la prueba, en el caso de la cistatina C de esta forma mejora la eficacia del sistema de gestión de calidad (Ver figura 3).
Ø
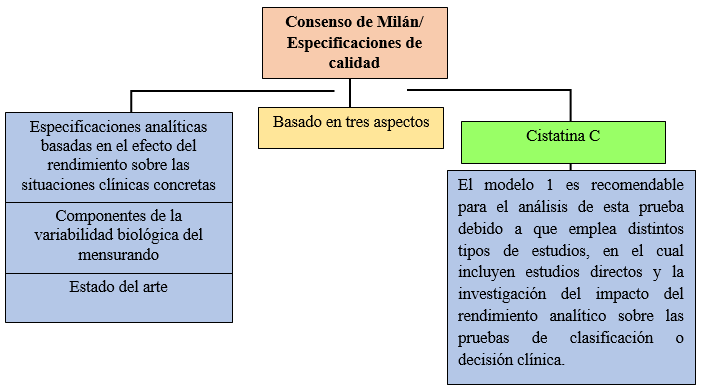
Figura 3. Especificaciones de la calidad analítica-Consenso de Milán
Ø Materiales de control de calidad: La selección correcta de estos materiales a concentraciones críticas o de decisión clínica le permite al analista prevenir el error aleatorio y eliminar el error sistemático del procedimiento, de esta forma le permitirá realizar un seguimiento del desempeño analítico para el uso previsto en los niveles más importantes para la cistatina C.(36)
Ø Tipos de materiales de control
Control de primera opinión: son aquellos materiales de control utilizados de la misma casa comercial que el reactivo empleado para la determinación de una prueba.(38)
Control de tercera opinión: son controles con procedencia diferente a los instrumentos y reactivos que se utilizan en el análisis de las pruebas.(38)
Para realizar análisis químicos de pruebas en el laboratorio como es el caso de la cistatina C distintas entidades como el Instituto De Estandarización De Los Laboratorios Clínicos (CLSI) específicamente en la Statistical Quality Control for Quantitative Measurement Procedures: Principles and Definitions (CLSI C24-A3), la Asociación Nacional de Autoridades de Pruebas, Australia (NATA), y el Sistema de Acreditación de Laboratorio de Malasia (LASM), recomiendan el uso de los controles de tercera opinión debido a que ayudan a identificar errores de reactivos, instrumentos o procedimientos que al ser inadvertidos pueden generar un error en la obtención de los resultados.(39)
Ø Establecimiento de media y desviación estándar: la media nos permite estimar de mejor manera el valor real de la cistatina C para un determinado nivel de control, es recomendable el n20 para establecer estas medias, y la desviación estándar ayuda a evaluar la precisión del sistema de prueba, por ello estas dos medidas le permiten al laboratorio establecer límites de decisión en las cuales se determina si el resultado del control es aceptable para este analito, además en el caso de que se presente un cambio de lote de control es necesario realizar un coeficiente de variación ponderado.(35)
· Determinación de exactitud: Bajo la norma ISO 17043 que se enfoca en la evaluación de la conformidad se debe acreditar el programa de evaluación externa de la calidad (EQAS) a partir de ello se determina adecuadamente las especificaciones de desempeño para el uso previsto del procedimiento de medida, mediante una comparación con medias robustas, en grupos segmentados: grupo par, métodos, todos, y estimar la exactitud de medición generalmente frente al grupo par. (35) Por ello la cistatina C resulta ser un biomarcador que proporciona una medida más exacta para estimar la función renal debido a que se filtra libremente por el riñón y evita unirse a proteínas plasmáticas, además al generar niveles elevados ayuda a identificar que existe un riesgo mayor para la enfermedad renal.(40)
· Datos de control de calidad: Es necesario aplicar reglas de control de calidad definidos para la cistatina C de acuerdo con el desempeño analítico estable del procedimiento de medición, de esta forma se verifica si la corrida analítica es aceptada o rechazada de acuerdo con la herramienta de planificación de calidad previamente seleccionada de acuerdo con el rendimiento de procedimiento.(34)
Post análisis: en esta etapa se lleva a cabo la revisión, reporte y liberación de los resultados obtenidos, el almacenamiento, retención, y desecho de las muestras analizadas.(41)
· Deltacheck: permite evaluar el porcentaje máximo de la variación que existe entre un resultado actual y uno ya obtenido según el analito analizado en este caso la cistatina C, el laboratorio clínico es el encargado de obtener estos coeficientes de variación delta a partir de un cv de control interno (42).
· Estrategia: estos límites de cambio en el laboratorio se pueden determinar a partir de percentiles de distribución poblacional o datos de la variabilidad biológica intraindividual.(42)
· Variabilidad intraindividual: dentro del laboratorio hace referencia a la fluctuación de la concentración que existe alrededor del punto de equilibrio entre los componentes de fluidos biológicos.
CONCLUSIONES
· La cistatina C ha demostrado ser una prueba útil al momento de relacionar los niveles que presenta con la gravedad de daño renal que puede llegar a tener un paciente, debido a que los valores que se obtengan de ella permiten estimar el fracaso renal agudo de forma precoz dado que su concentración sérica suele elevarse dentro de las 36 a 48 horas a comparación de otras pruebas.
· Además este biomarcador aporta de forma significativa al diagnóstico temprano de daño renal, en personas asintomáticas donde se presentan niveles normales de creatinina y una baja tasa de filtrado glomerular (TFG) esta prueba es confiable para estimar el filtrado glomerular real, por ello puede ser utilizada como una prueba complementaria en pacientes con riesgo a desarrollar insuficiencia renal crónica.
· Por otra parte al presentar una mejor exactitud la cistatina C es considerado como un indicador pronóstico de daño renal importante ya que en el área de salud permite obtener un diagnóstico más preciso en cuanto a esta enfermedad.
· Finalmente dentro de laboratorio clínico un parámetro indispensable es el análisis de la cistatina C dado que es fundamental para el diagnóstico y pronóstico de la enfermedad renal, esta prueba además de ser rápida, no invasiva y automatizada presenta una mejor exactitud y mayor sensibilidad.
REFERENCIAS BIBLIOGRÁFICAS
1. National Institutes of Healt. Insuficiencia renal. [cited 2023 Nov 5]. Available from: https://www.cancer.gov/espanol/publicaciones/diccionarios/diccionariocancer/def/insuficiencia-renal
2. Stanford Medicine Children’s Health. Descripción general de la insuficiencia renal. [cited 2023 Nov 5]; Available from: https://www.stanfordchildrens.org/es/topic/default?id=overview-of-renal-failure-in-children-90-P06204
3. Abarca Rozas B, Mestas Rodríguez M, Widerström Isea J, Lobos Pareja B, Vargas Urra J. A current view on the early diagnosis and treatment of acute kidney failure. Medwave. 2020 Jun 1;20(5).
4. Soledispa Jiménez William Gregorio. Insuficiencia renal aguda y factores de riesgo en pacientes covid – 19. Pentaciencias. 2022;4:484498.
5. Urbina Aucancela CY, Urbina Aucancela KD. Cistatina C y Creatinina Sérica como predictor de falla renal aguda en pacientes críticamente enfermos. Recimundo. 2021 Oct 24;5(4):132–42.
6. García-Maset R, Bover J, Segura de la Morena J, Goicoechea Diezhandino M, Cebollada del Hoyo J, Escalada San Martín J, et al. Documento de información y consenso para la detección y manejo de la enfermedad renal crónica. Nefrología. 2022 May;42(3):233–64.
7. Diaz M, Gómez L, Robalino M. Comportamiento epidemiológico en pacientes con enfermedad renal crónica terminal en Ecuador Epidemiological behavior on patients with terminal chronic kidney disease from Ecuador. 2018. p 1-13.
8. Villafuerte Fernández AA, Pazmiño Villao AJ, Romero Urréa HE, Yuquilema-Cortez MB, Salas Alvarado JA. Validación de instrumentos para evaluar la calidad de vida del adulto mayor con insuficiencia renal crónica. Más Vita. 2022 Jul 1;4(2):293–303.
9. Organización Mundial de la Salud. Las 10 principales causas de defunción. 2020 [cited 2023 Oct 29]. Available from: https://www.who.int/es/news-room/fact-sheets/detail/thetop-10-causes-of-death
10. INEC. Estadísticas vitales-registro estadístico de defunciones generales de 2020. 2020. p 1-33.
11. Pazmiño Villao AJ, Villafuerte Fernández AA, Romero Urréa HE, Vaquero Gonzales NB, Llanos Oquendo ER, Cherrez Paredes IC. Diagnóstico de enfermería del estado emocional en pacientes con insuficiencia renal crónica durante su tratamiento. Más Vita. 2022 Jul 1;4(2):64–76.
12. Reyes Correa Diego Fernando. Perfil renal y estilo de vida en adultos de américa latina. Pentaciencias. 2022;443–62.
13. Gahona Villegas JR, Reyes Jurado P, Prado Cabrera AS, Meza Rodríguez KM, Benítez Kellendonk CH. Descripción y análisis de la tasa de incidencia y prevalencia de pacientes en terapia de reemplazo renal en Ecuador. Metro Ciencia. 2023 Jun 30;30(2):35–40.
14. KDIGO. KDIGO 2023 clinical practice guideline for the evaluation and management of chronic kidney disease public review draft. 2023. p1-339.
15. Zambrano Jivania. Proteínas séricas y concentración de electrolitos en pacientes con insuficiencia renal crónica. Pentaciencias. 2023;25–35.
16. López-Heydeck SM, López-Arriaga JA, Montenegro-Morales LP, Cerecero-Aguirre P, Vázquez-De Anda GF. Laboratory analyses for early diagnosis of chronic kidney disease. Vol. 78, Revista Mexicana de Urologia. Sociedad Mexicana de Urologia. Colegio de Profesionistas A.C.; 2018. p. 73–90.
17. Legton MG, Mendoza NA. Cistatina c, urea y creatinina como indicador pronóstico de daño renal. MQRInvestigar. 2023 Jul 12;7(3):628–46.
18. Solís M, Benavides G, Vásconez E, Campoverde A. Correlación de cistatina “C” y creatinina sérica frente al filtrado glomerular en pacientes con nefropatía diabética. Cambios. 2020;22–8.
19. Sociedad Colombiana de Patología Clínica. Inmunoensayo turbidimétrico para la detección de cistatina C. 2014. p 575-578.
20. Fleta Zaragozano J, Pilar Samper Villagrasa M, Bueno Lozano M, Nuviala Mateo R, Luis Olivares López J. Cistatina C: filtración glomerular y enfermedad cardiovascular Artículo Original. 2018. p 61-66.
21. Alcívar Vásquez Juan Manuel, Puig Gilbert Carlos Alberto, Lama Jeany Wong, Flor Rodríguez Miguel Angel. Determinación de Cistatina C como marcador de función renal en pacientes normoalbuminúricos con Diabetes Mellitus tipo 2. Estudio Multicéntrico. Rev sen. 2021;21–7.
22. Coronado Herrera Yohana. Revista Electrónica de PortalesMedicos.com. 2022 [cited 2023 Nov 11]. Cistatina C y Creatinina: marcadores de función renal en pacientes tratados con Cisplatino. Available from: https://www.revistaportalesmedicos.com/revista-medica/cistatina-c-y-creatinina-marcadores-de-funcionrenal-en-pacientes-tratados-con-cisplatino/
23. Darias D. Intervalo de referencia para la cistatina C en una muestra de población adulta cubana Reference Interval for Cystatin C in a Sample of Adult Cuban Population. :14– 25. Available from: https://revfinlay.sld.cu/index.php/finlay/article/view/698
24. Ramírez López L, Albarracín Suárez L, Castillo Zaraza D, Bueno Sánchez J, Aguilera Becerra A. Cystatin C vs conventional markers of renal function: an update. Salud Uninorte. 2020 Apr 13;35(1):110–32.
25. Betancourt Gori, Ollarves Carrero María Antonieta, Verlezza SMF. Utilidad clínica de la cistatina C como marcador precoz de enfermedad renal crónica. [cited 2023 Nov 26]; Available from: https://pesquisa.bvsalud.org/portal/resource/pt/lil-772210?lang=en
26. Álvarez E, Tortorici M, Cañizares B. Diagnóstico precoz y estadios de la enfermedad renal diabética albuminuria e índice de filtración glomerular estimado. 2020;
27. García J. “Estudio de la cistatina C plasmática y urinaria en medicina canina: enfermedades renales y no renales.” 2018. p 1-250.
28. Benavides Couto A, Rodríguez Jiménez Y, González Borges D, Luisa I, Serrano M, Hernandez Palet I, et al. Use of Cystatin C Biomarker in Patients with Possible Renal Failure. Revista Finlay [Internet]. 2019;2–10. Available from: https://revfinlay.sld.cu/index.php/finlay/article/view/717
29. Rosell D, Gil L, Herrera Y, Reyes A, Rosell T. Cystatin c: useful marker in renal damage in pathologies and/or by the use of drugs. Biol [Internet]. 2022;53(3).
30. Medical laboratories — Requirements for quality and competence. ISO 15189:2022(es) Laboratorios clínicos — Requisitos para la calidad y la competencia. 2022 [cited 2023 Nov 12]; Available from: https://www.iso.org/obp/ui/#iso:std:iso:15189:ed4:v1:es:term:3.8
31. Ministerio de Salud Pública. Manual de proceso preanalítico. 2018. p 1-53.
32. Organización Panamericana de la Salud. Empaque y transporte de muestras procedimiento integral para gestión de una muestra posiblemente contaminada con microorganismos muy peligrosos OPS. 2022. p 1-12
33. González Álvarez Yusimí, Carrazana Masiel, Pérez Lutgarda, Alemán Adialys. Cistatina C como marcador precoz de daño renal en pacientes con Diabetes Mellitus II. Cuba Salud. 2022;1–9.
34. Servicio de Acreditación Ecuatoriana. Criterios Generales R02 para la acreditación de laboratorios clínicos según la norma ISO. 2022. Available from: www.acreditacion.gob.ec
35. Westgard JO, Migliarino GA. Edición Wallace Coulter Sistemas de Gestión de la Calidad para el Laboratorio Clínico. 2014. 1–268.
36. Westgard JO, Barry PL, Ehrmeyer SS, Plaut D, Quam EF, Statland BE, et al. Prácticas Básicas de Control de la Calidad 3 a Edición Capacitación en Control Estadístico de la Calidad para Laboratorios Clínicos. 2010. p 1-393.
37. Sistemas de gestión de la calidad-Requisitos Quality management systems-Requirements. 2015. Available from: www.iso.org
38. Migliarino GA. Actualizaciones en el aseguramiento de la calidad analítica para pruebas de tamizaje. Revista Mexicana de Medicina Transfusional. 2023;15(S1):s20-21.
39. López C. La importancia de procesar controles de calidad internos de tercera opinión imparciales independientes. 2018. 1-7p.
40. Lambis A, Roldan M, Martínez L. Enfermedad renal crónica: Cistatina C como marcador diagnóstico. Chronic kidney disease: Cystatin C as a diagnostic marker. :2463–1426.
41. Castro-Castro MJ, Sánchez-Navarro L. Estimation of change limits (deltacheck) in clinical laboratory. Advances in Laboratory Medicine. 2021 Sep 1;2(3):417–23.
42. Ghisolfi C. Variabilidad Biológica. Su importancia en la interpretación de resultados en el laboratorio clínico. 2019. 1-2p.
FINANCIACIÓN
Los autores no recibieron financiación para el desarrollo de la presente investigación.
CONFLICTO DE INTERESES
No existe conflicto de interese.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Chugcho Aguagallo Alexandra Estefanía.
Investigación: Chugcho Aguagallo Alexandra Estefanía.
Metodología: Chugcho Aguagallo Alexandra Estefanía.
Administración del proyecto: Moina Veloz Álvaro Paul.
Supervisión: Moina Veloz Álvaro Paul.
Redacción – borrador original: Chugcho Aguagallo Alexandra Estefanía.
Redacción – revisión y edición: Chugcho Aguagallo Alexandra Estefanía.